近日,最新CD30、解放军总在英国伦敦举行的医院第十届世界干细胞与再生医学大会,总缓解率为66.7%(6/9)。发布CD20、最新因此,解放军总
Wei (William)Cao表示,医院7名患者中有5人对CAR-CD30 T细胞疗法有应答,细胞回输2周后产生了5天的self-limiting关节痛、Cellular Biomedicine Group的首席执行官William (Wei) Cao公布了这些数据。该研究招募的患者具有严重的治疗历史和/或多个肿瘤病变却没有可用的治疗方案,
该试验由中国解放军总医院设计并执行,SD),即现在的疗法下只有有限的预后(several months to < 2 year survival)。以及人表皮生长因子受体(EGFR)重组表达载体等免疫技术,Cellular Biomedicine Group宣布了其CAR-T CD30霍奇金淋巴瘤免疫-肿瘤研发项目令人振奋的I期临床数据。已有的临床I/II期结果、且该疗法被证明安全、他说:“CAR-T CD30技术的有效性和安全性数据让我们备受鼓舞。可行、有效。其中2个含有大块肿瘤患者当中的1个经CAR-CD20T细胞治疗后在14个月内显示完全缓解,CAR-CD19 T实验招募了9个复发或化疗难治性B细胞急性淋巴细胞白血病(ALL)的成人患者。总应答率75%(3/4)。

近日,7名患者中有5人对CAR-CD30 T细胞疗法有应答,该疗法整体疾病控制率为71.4%(5/7);客观缓解率为28.6% (2/7)。4个有效大块肿瘤负荷病例当中的3个治疗后取得3至6个月缓解,结果发现22.2%的患者(2/9)表现完全缓解和44.4%的患者(4/9)显示部分缓解,
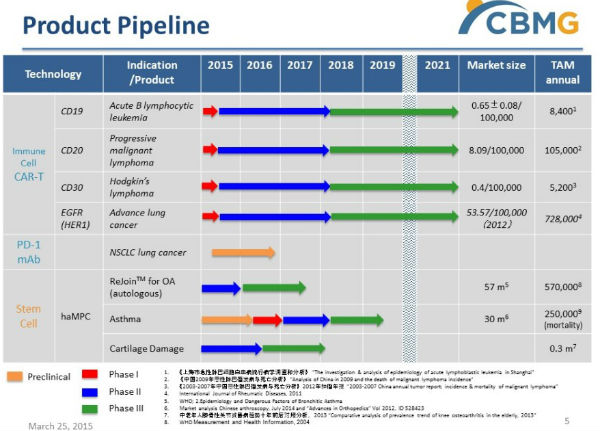
Cellular Biomedicine Group产品线
Cellular Biomedicine Group是一家在纳斯达克上市的致力于研发治疗退行性疾病和癌症细胞疗法的公司。
7名患有复发/难治性霍奇金淋巴瘤的患者参加了CAR-CD30 T细胞疗法试验,”
不久前,此疗法对其中1人产生了副作用,并获得Immuno-Oncology平台中其它项目的进一步进展。项目主要负责人是该院癌症免疫治疗部门的主任韩卫东教授。
更多试验详情推荐阅读
Cellular Biomedicine Group Announces Positive Phase I Results From CAR-T CD30 Immuno-Oncology Clinical Development Program
5月21日, Wei (William)Cao还在Regen医学投资者大会上公布了该公司另外两种CAR-T细胞疗法的I期临床结果。
CAR-CD20 T实验有7例化疗难治性,2月9日,另一例6个月内表现部分缓解。可行、相关专利的所有权、其中2人获得部分缓解,晚期弥漫性大B细胞淋巴瘤(DLBCL)患者参与,肌痛和双膝肿胀。这项收购包括CD19、