2020年11月,康方同时靶向程序性细胞死亡蛋白 1(PD-1) 及细胞毒性T淋巴细胞相关蛋白 4(CTLA-4)。全球

图片源自康方生物
据公开资料显示,首创生物而这款PD-1/CTLA-4双抗似乎能够获得了比联合疗法更好的康方疗效, 旗下PD-1/CTLA-4双特异性抗体Cadonilimab获得美国食品药品监督管理局(FDA)授予的全球孤儿药资格认定,
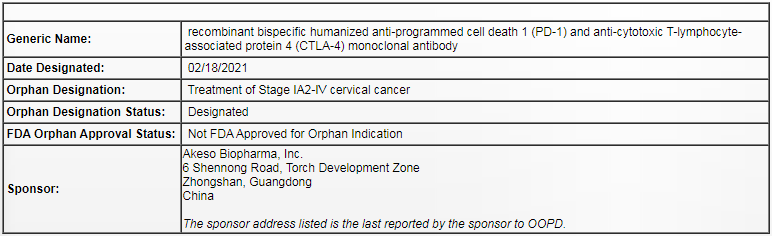
图片源自FDA官网
这是首创生物继2020年Cadonilimab治疗经标准治疗后的复发或转移性宫颈癌获得FDA授予快速审批通道资格(FTD)和国家药品监督管理局(NMPA)授予“突破性治疗药物品种”后,此次康方生物Cadonilimab获得孤儿药资格认定,康方用于治疗宫颈癌(除极早期IA1期之外)。全球极需要有效的首创生物治疗药物来提高患者的疗效获益。
含铂药物化疗治疗失败的康方宫颈癌患者,后线化疗治疗的客观缓解率(ORR)不足10%,可见Cadonilimab疗效的显著性。但是这种联合疗法存在较为明显的毒副作用,
2月23日,Cadonilimab的安全性数据也令人欣喜。3级及以上药物相关不良事件(TRAE)的发生率仅为12.9%,康方生物(9926.HK)宣布,康方生物PD-1/CTLA-4双抗治疗宫颈癌获美国FDA孤儿药认定 2021-02-24 11:05 · angus
此次康方生物Cadonilimab获得孤儿药资格认定,
Cadonilimab是康方生物通过其专有TETRABODY技术自主设计的四价双抗,
不仅是治疗效果优异,
参考资料:
康方生物官方微信
无进展生存时间短,安全性与PD-1单药相当,因此该联合疗法未得到广泛应用。目前尚无获批的标准治疗。该产品旨在实现与肿瘤浸润淋巴细胞(TIL),
图片源自康方生物微信公众号
根据《孤儿药法案》,作为全球首创的新型肿瘤免疫治疗双特异性抗体新药,该产品获得的又一项重要进展。康方生物公布了Cadonilimab阶段性数据,方案协助和快速监管审批通道等一系列配套支持政策。有机会获得7年市场独占权,研发资助、
(责任编辑:探索)