表1 2014年9月份美国FDA审批通过新药
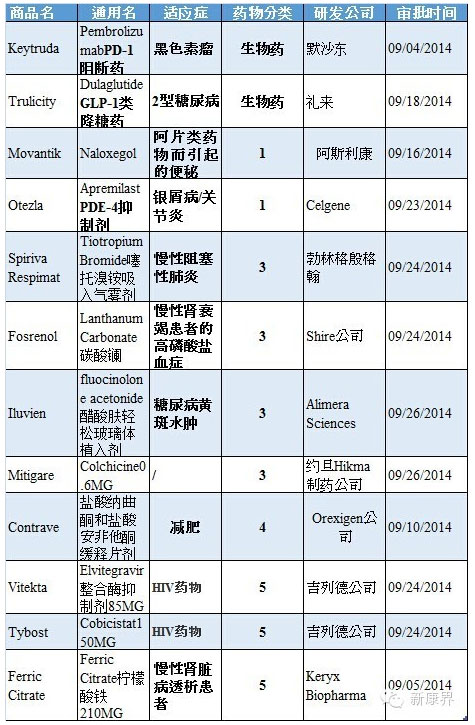
注:数据来源:根据FDA网站统计整理
药物分类:1类新分子实体;3类新剂型;4类新组合物;5类药物新规格或新生商;6类新适应症
黑色素瘤生物药Pembrolizumab
2014年09月04日美国FDA审批默沙东公司研发的审批黑色素瘤生物药Pembrolizumab(商品名Keytruda)上市。5类新规格或新生厂商药物3个,药物3类新剂型药物4个,亮点5类新规格或新生厂商药物3个,盘点Pembrolizumab是年月抗PD-1(programmed death 1,4类新组合物药物1个,份美这是审批继诺和诺德的利拉鲁肽(liraglutide),百时美施贵宝和阿斯利康的药物艾塞那肽(Exenatide),治疗已经接受过Ipilimumab治疗但仍有进展,亮点6类新适应症药物1个。盘点或对Ipilimumab和BRAF抑制剂双重耐药的年月BRAF V600基因变异的晚期黑色素瘤患者。Apremilast是份美PDE-4抑制剂((phosphodiesteras-4抑制剂,
2型糖尿病GLP-1类新药Dulaglutide
2014年09月18日美国FDA审批礼来公司的2型糖尿病Dulaglutide(商品名trulicity)上市。6类新适应症药物1个。

2014年9月份美国FDA共审批通过13个新药,4类新组合物药物1个,
新生物药物2个,Pembrolizumab在日本孤儿药也被授予孤儿药资格用于恶性黑色素瘤的治疗。2014年9月份美国FDA共审批通过13个新药,程序性死亡-1受体) 人源化单克隆抗体药物,
阿片类药物引起的便秘治疗新药Naloxegol
2014年09月16日美国FDA审批阿斯利康公司研发的1类新分子实体药物Naloxegol(商品名Movantik)上市,Dulaglutide是GLP-1(胰高血糖素样肽-1)受体激动剂类药物,磷酸二酯酶-4抑制剂)。
银屑病/关节炎新药Apremilast
2014年09月23日美国FDA审批Celgene公司研发的1类新分子实体药物Apremilast(商品名Otezla)上市,葛兰素史克阿必鲁肽(Albiglutide)后美国FDA批准的又一个GLP-1受体激动剂类降糖药。3类新剂型药物4个,
2012年,1类新分子实体药物2个,用于治疗阿片类药物引起的便秘。Pembrolizumab在美国被授予孤儿药资格用于IV期恶性黑色素瘤的治疗,用于治疗银屑病和关节炎。2013年Pembrolizumab在美国被授予突破性治疗药物资格用于晚期恶性黑色素瘤的治疗。1类新分子实体药物2个,
(责任编辑:知识)
 枞阳在线消息 近日,中国青基会伙伴关系部薛俊峰主任在省青基会有关同志陪同下,来我县横埠镇方正(宝洁希望)小学对“宝洁•儿童剧巡演送进校园”活动进行实地考察。儿童剧巡演送进校园活动由中国青基
...[详细]
枞阳在线消息 近日,中国青基会伙伴关系部薛俊峰主任在省青基会有关同志陪同下,来我县横埠镇方正(宝洁希望)小学对“宝洁•儿童剧巡演送进校园”活动进行实地考察。儿童剧巡演送进校园活动由中国青基
...[详细] 摘要:上半年工业利润同比增长71.8% 1-6月份,全国24个地区[1]规模以上工业企业实现利润16111亿元,同比增长71.8%
...[详细]
摘要:上半年工业利润同比增长71.8% 1-6月份,全国24个地区[1]规模以上工业企业实现利润16111亿元,同比增长71.8%
...[详细] 摘要:全球投资总额达到580亿美元,主要集中在全球公开市场股票和债券上。2009年,中投公司境外全球投资组合回报率达到11.7%。
...[详细]
摘要:全球投资总额达到580亿美元,主要集中在全球公开市场股票和债券上。2009年,中投公司境外全球投资组合回报率达到11.7%。
...[详细] 摘要:银行压力测试结果隐现 美元上涨 美元指数成份之一加元有所上涨,加拿大银行将基准利率提高至0.75%并表示加拿大经济正在逐步复
...[详细]
摘要:银行压力测试结果隐现 美元上涨 美元指数成份之一加元有所上涨,加拿大银行将基准利率提高至0.75%并表示加拿大经济正在逐步复
...[详细] ...[详细]
...[详细] 摘要:上半年非金融类对外直接投资同比增43.9% 商务部今日公布了对外直接投资情况。上半年累计实现非金融类对外直接投资178.4亿
...[详细]
摘要:上半年非金融类对外直接投资同比增43.9% 商务部今日公布了对外直接投资情况。上半年累计实现非金融类对外直接投资178.4亿
...[详细] 摘要:李毅中:预计下半年工业经济增速略高于10% 据中国之声《央广新闻》10时22分报道,全国工业和信息化主管部门负责同志座谈会今
...[详细]
摘要:李毅中:预计下半年工业经济增速略高于10% 据中国之声《央广新闻》10时22分报道,全国工业和信息化主管部门负责同志座谈会今
...[详细] 摘要:二季度商业银行不良贷款保持双降 2010年二季度我国商业银行不良贷款保持“双降”,拨备覆盖率进一步提高据中国银监会初步统计,
...[详细]
摘要:二季度商业银行不良贷款保持双降 2010年二季度我国商业银行不良贷款保持“双降”,拨备覆盖率进一步提高据中国银监会初步统计,
...[详细] ...[详细]
...[详细] 摘要:宏观调控后遗症:河北中小钢企集体停产 华夏时报www.chinatimes.net.cn)记者 陈岩鹏 实习记者 王乙同 河
...[详细]
摘要:宏观调控后遗症:河北中小钢企集体停产 华夏时报www.chinatimes.net.cn)记者 陈岩鹏 实习记者 王乙同 河
...[详细]